Открытые учеными химические источники электрического тока прочно вошли в практику. Удобные и компактные, они и теперь продолжают надежно трудиться, в том числе и в самой наисовременнейшей аппаратуре.
В наиболее популярном марганцево-цинковом элементе с солевым электролитом (см. рис.) в качестве отрицательного электрода (минуса) используется цинк Zn, а положительным (плюсом) является порошкообразный диоксид марганца МnO2 в смеси с углем или графитом (для уменьшения сопротивления). Электролитом же служит паста, составленная из нашатыря NH4Cl, крахмала и некоторых других веществ (деполяризаторов). В результате химических реакций из отрицательного электрода уходят положительные ионы цинка (их отбирает содержащийся в нашатыре атом хлора). Одновременно с этим положительные ионы NH4+, которые появляются в электролите из-за его самопроизвольного химического распада, отбирают свободные электроны из диоксида марганца, и появляется значительный положительный заряд.
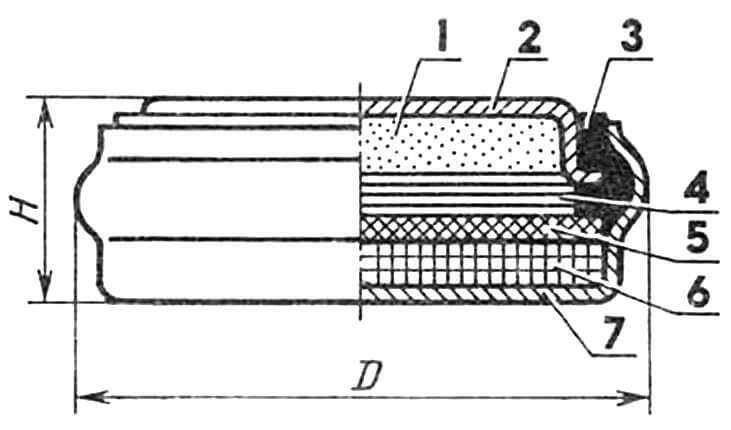
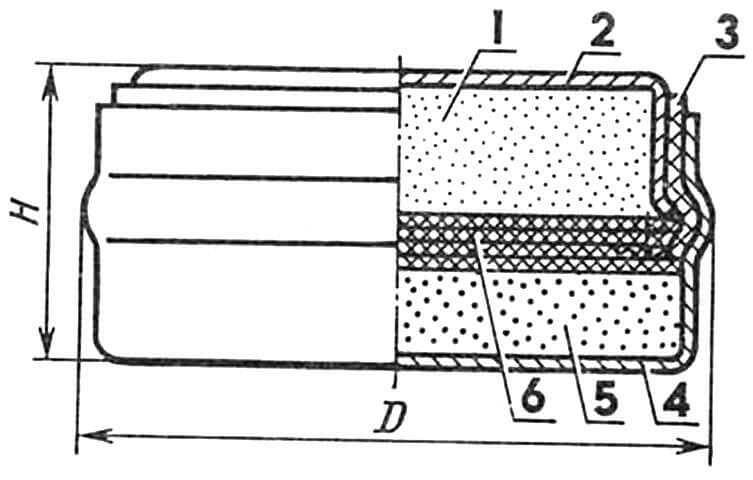
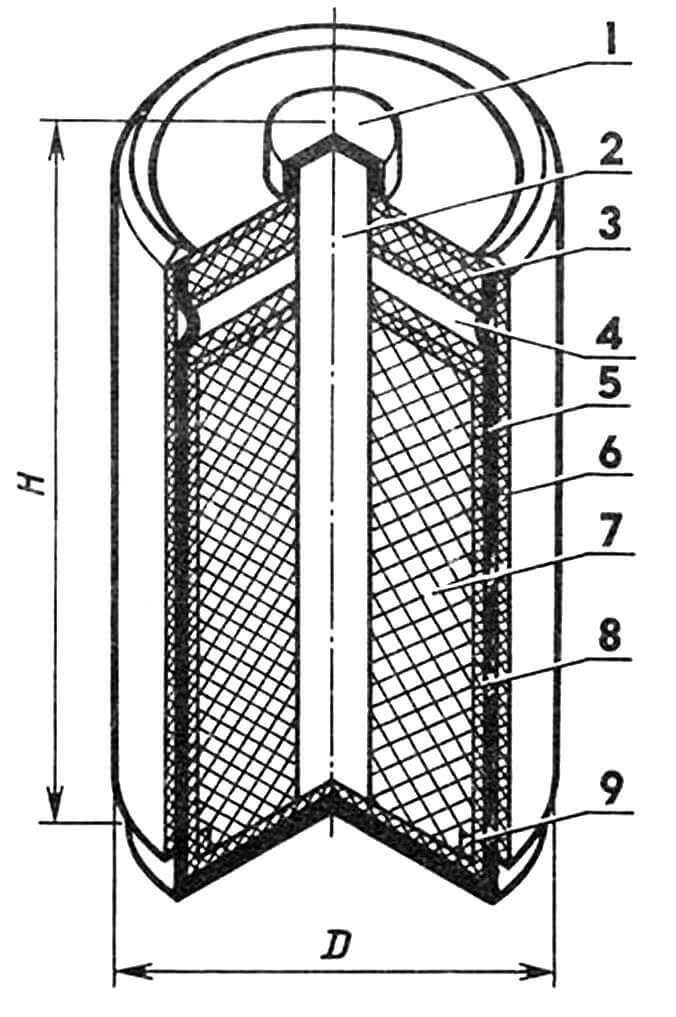
В результате на полюсах гальванического элемента образуется разность потенциалов, величину которой каждый, наверное, пытался в свои детские годы «оценить на вкус», мгновенно прикасаясь языком к выводам со знаком «плюс» и «минус».
Следует, однако, отметить, что процесс интенсивного роста потенциалов в никуда не подсоединенном гальваническом элементе идет, увы, не до бесконечности. Он вскоре неминуемо прекратится, так как у химических реакций не будет «хватать сил» на преодоление отталкивающего действия скапливающихся на электродах избыточных зарядов.
Но стоит подключить «нагрузку» (например, мини-электролампу), как через нее потечет ток, «убирая» с одного электрода положительные ионы, а с другого — свободные электроны. В гальваническом элементе вновь активизируются описанные ранее окислительно-восстановительные реакции, поставляя электродам избыточные заряды. И так будет продолжаться до тех пор, пока хватит «химического сырья» или пока не разомкнут электрическую цепь, отключив «нагрузку».
Еще А. Вольта заметил, что значительно лучшими эксплуатационными характеристиками обладают элементы не с солевым, а с более дорогим щелочным электролитом. Естественно, промышленность не преминула наладить и их производство. Причем как марганцево-цинковых, так и ртутно-цинковых (см. таблицу в № 11’94 и иллюстрации данного номера). Выпускаются также специальные литиевые гальванические элементы, но из-за высокой стоимости и по ряду других причин — не столь массово.
Приобретенные элементы любых типов и модификаций имеют неприятное свойство. Со временем они начинают «стареть». Уверен: в любом доме найдутся вышедшие из строя, высохшие гальванические элементы с частично разъеденными стенками стаканов (корпусов), разряженные полностью или частично. Участь таких обычно незавидная — их попросту выбрасывают.
Подобная расточительность (особенно в период неуклонного роста в стране дороговизны и дефицита) вряд ли оправдана. Ведь можно (хотя бы частично) дать старым или, казалось бы, вконец уже разряженным гальваническим элементам «вторую жизнь». Тем более что методика восстановления работоспособности таких источников электропитания давно уже доведена до совершенства опытными радиолюбителями.
Прежде всего стоит очистить поверхность стакана (корпуса) от наклеек, потеков компаундной массы, засохших отложений солей, заблаговременно опустив их в воду. Затем в стенке проделывают шилом два отверстия, стараясь не задеть мешочка с диоксидом марганца (как, впрочем, и уплотнения): одно — в 10 мм от верхнего края стакана, а другое — отступив примерно 3 мм от донышка.
Теперь предстоит насытить элемент влагой. Точнее — 15-процентным раствором хлористого аммония, предварительно позаботившись о том, чтобы компаунд в него не попадал, не загрязнял (заизолировать можно, натянув, скажем, отрезок резиновой перчатки и т. п.).
Выдержав элемент в растворе при комнатной температуре, переходят к циклическому режиму: нагреву до 90° С с последующим охлаждением. Причем делают это, поместив емкость с одним или несколькими восстанавливаемыми источниками тока, залитыми раствором, в водяную баню. Нагрев-охлаждение повторяют несколько раз, пока из обоих отверстий в стакане не прекратится (при очередном нагреве) частичное выделение пузырьков с характерным запахом аммиака.
Избытку раствора дают стечь из охлажденных элементов и… ставят последние на зарядку, расположив их горизонтально, отверстиями вверх. При достижении 1,9 В или когда напряжение на заряжаемом источнике тока стабилизировалось (после получасовой выдержки не снижается более чем на 0,2 В), процесс восстановления можно считать в целом законченным. Нужно лишь, дождавшись прекращения выхода газа из отверстий (а это занимает обычно 3—4 дня), загерметизировать корпус (например, затычкой из спички) и покрыть слоем клея для металла. Ну а чтобы до этого электролит не высыхал, временно залепить отверстия пластилином.
Промышленность наладила в последнее время выпуск довольно широкого ассортимента зарядных устройств. Есть среди них и специальные, предназначенные для подзарядки гальванических элементов и аккумуляторов. Любители же мастерить все своими руками могут собрать аналогичные устройства и сами. Тем более что и добротных схем для сборки существует множество.
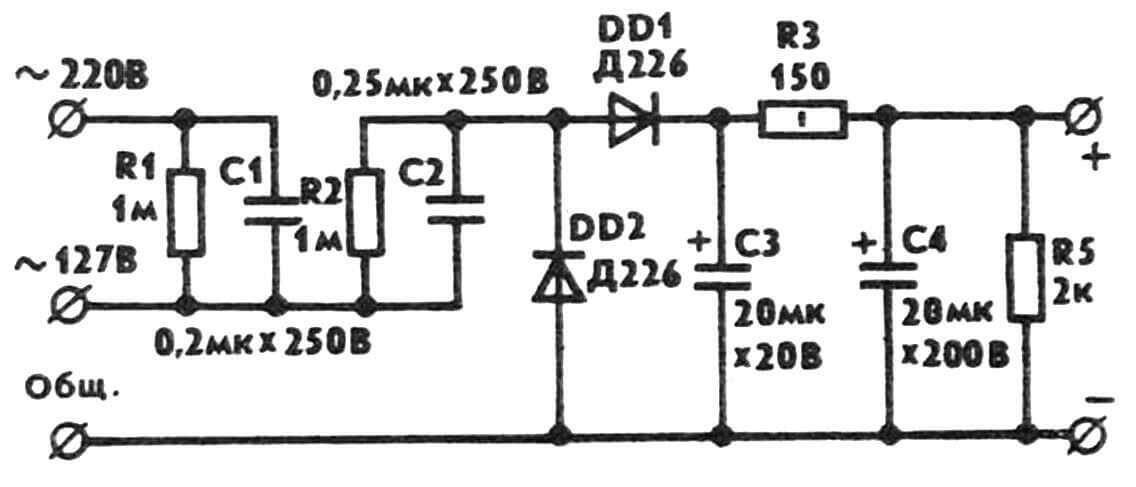
Начинающим же радиолюбителям можно порекомендовать давнюю, но достаточно эффективную разработку. Дефицитных и дорогостоящих деталей для ее осуществления (см. принципиальную электрическую схему) не потребуется. Как, впрочем, и печатной платы — выручит здесь опять-таки навесной монтаж. Деталей-то в схеме по пальцам пересчитать можно. И наладки особой тоже не требуется.
Только вот проверять работоспособность устройства «на язык», как когда-то в детстве батарейку, нельзя: ведь в сети — высокое напряжение, опасно для жизни!
Н. КОЧЕТОВ

